2008年8月11日
ゼミ担当教授:井原良訓
報告:尾形正宏
はじめに
さあて,今日もまた「化学」の世界です。
今日のテーマは<色>。ゼミ担当の井原先生が<色>の研究をしていらっしゃるそうで,実験室に持ってこられた「子ども用のスプーン」も,温度によって変色するものでした。こういうのを集める教授って,それだけで楽しそうです。
子どもでなくても,色が変わるというだけで,気分は浮き浮きしてしまいます。残念ながら,なぜこういう変化が起きるのかは理解できませんが,それはヨウ素デンプン反応とて同じこと。BTB液の変色反応だって,なんであんな色になるのか知らないですからね。ま,それでもちゃんと理科の教師ができるのだから…
今回は,参加者がみんな同じ実験をするのではなく,いくつかの実験から選んで,それを見合うことにしました。

塩化コバルトで温度変色テープの製作(温度による変化)
まず私がやったのは,「塩化コバルト」という薬品を使って,「サーモテープ」の変わりのものを作ることです。
今(2008年現在)市販されている(ということは理科室にある)サーモテープには,実は水銀化合物が使われているそうです。学校では,使った後であまり気にせずにゴミとして捨てているのではないでしょうか。これは危険です。捨てないまでも,子どもたちが普通に扱っていることを考えると,変わりに安全なものがあるのなら,それで代用した方がいいでしょう。そんなものを教えてもらいました。
【材料】
塩化コバルト(Ⅱ)・6水和物,乳鉢,ラミネートシート,両面テープ,ステンシルハケ(綿棒でもよい)
【作り方】
1 ラミネートシートを1.5cm~2cm幅に切断する。
2 両面テープの片面をラミネートシートに貼り付ける。
3 塩化コバルトを乳鉢ですりつぶす。
4 3のものを2の上に均質にステンシルハケで貼り付ける。
5 低温でパウチする。


【解説】
両面テープにつける固体の塩化コバルト(CoCl2・6H2O)はピンク色ですが,50度以上になると水を失って青色の無水物となります。これは何度も使えます。冷えるとちゃんとピンクに戻ります。
実は,この講座のあと,秋の石川県教育研究集会理科部会に出席しました。そのとき,「この方法でサーモテープ」を作るという発表があり,その発表者がこれを考え出したそうです。
「特許を取ればいいのに…」とみんなで言っていました。
理科部会では,休憩時間にみんなでテープを作ってみました。熱の伝わり方の授業で力を発揮するようです。
変色振動反応1 (酸化・還元反応による変化)
これはおもしろかったです。
なんせ,フラスコに入れて,激しくふるだけで色が変わるのです。で,フリフルするのをやめると,また元に戻るんです。なぜ色が変わるのかは,下の【解説】を読んでください。

【材料】
ビーカー(300ml),平底フラスコ(300ml),薬サジ,ブドウ糖,水酸化ナトリウム,インジゴカルミン
【作り方】
1 ビーカーに水250mlを入れ,3gのブドウ糖を溶かす。
2 さらに5gの水酸化ナトリウムを加えて溶かし,液を平底フラスコに移しかえる。
3 インジゴカルミンを少量(薬サジの小さい方)加えると,黄色の溶液となる(Aの写真)。
4 フラスコをゆっくり穏やかに振ると液は赤色(Bの写真)に,さらに激しくふると液は緑色になる(Dの写真)。




【解説】
酸化還元による色の変化で,液性による変化ではありません。
インジゴカルミンをアルカリ性下でブドウ糖により還元すると黄色になります。
フラスコを振って空気中から酸素を取り込みやすくすると,液は酸化されて緑色になるのだそうです。
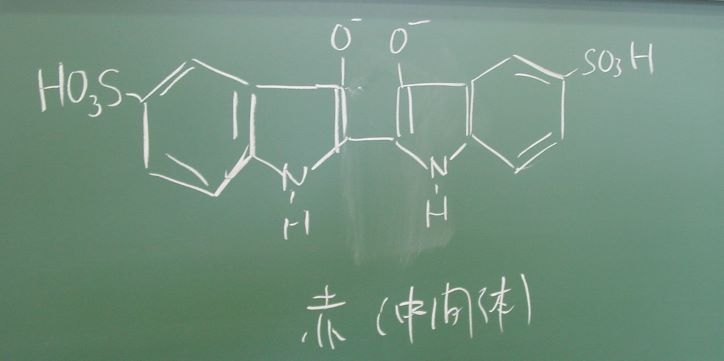
それらの反応の中間色として赤色の状態があるのです。
放置すればインジゴカルミンは還元されて黄色になり,繰り返し色の変化をみることができます。
変色振動反応2 (酸化・還元反応による変化)
これもおもしろい反応でした。ある液を混ぜて攪拌すると勝手に色が変化していくのです。その変化は,4~5回ほど続きました。そのあとは全く変化しなくなります。
この変化もまた,私にとってはブラックボックス的変化でしかありませんが,見ていても飽きませんでした。一応説明されるのですが,やっぱり不思議です。
【材料】
ビーカー(500ml,300ml,100ml),ガラス棒
過酸化水素水,ヨウ素酸カリウム,過塩素酸,マロン酸,硫酸マンガン四水和物,可溶性デンプン,
【作り方】
A液…3%過酸化水素水
B液…ヨウ素酸カリウム8.6g,70%過塩素酸2.7mlを水に溶かして200mlとする。
C液…マロン酸3.1g,硫酸マンガン四水和物0.7g,及び可溶性デンプン0.2gを溶かして200mlとする。
1 200mlのビーカーに,A,液,B液,C液をそれぞれ30mlずつ混ぜて攪拌を続ける。
2 そうすると溶液の色は,無色→薄黄色→金色→濃青色→無色…の変化を,4,5回繰り返す。




【説明】
ヨウ素とヨウ素イオンの間,及びマンガン2価と3価間での酸化還元反応が関わっていることは間違いないが,反応の詳細については不明だそうです。
今の化学をもってしてもわからないことがあることにビックリです。
消える水中カラーシャボン玉 (酸化・還元反応による変化)
これもまたおもしろい変化でした。水中で色つきのシャボン玉が漂っているのですから。写真でその様子を感じられるのかどうか…。実物の雰囲気が伝わりますか?

【材料】身近なものでできますよ
ビーカー(200ml),台所用中性洗剤,ストロー
【水に浮かぶシャボン玉の作り方】
1 200mlビーカーに水を入れ台所用洗剤を適量(100mlあたり3~5滴)加え,ストローで泡立てないように混ぜて石けん水を作る。
2 ストローを石けん水に2~3cm差しくみ,指でストローの口をふさぐ。
3 そのまま石けん水からストローを抜き,水面上5mm~1cmの高さからふさいでいた指を離して石けん水を落とすと,水中シャボン玉ができる(ちょっとコツがありますが,何度かやっているとできることが多くなります)。
4 ストローで落とす方の液体をあらかじめフェノールフタレインやBTBなどの指示薬で色づけしておくとカラー水中シャボン玉となる。このとき,ビーカー側の石けん水を若干酸性にしておくと,シャボン玉が割れた後の色水がゆっくり拡散しながら消えていく。
5 石けん水に食塩や砂糖を加えて密度を高くすれば,水中に漂うシャボン玉ができる。
【解説】
シャボン玉の中心は液滴で,そのまわりには空気の薄膜ができています。つまり,空気中の普通のシャボン玉と,気体・液体を逆転した構造になっているのです。
同一試薬で異なる発色をする試薬の調整 (酸化・還元反応による変化)
【材料】
ビーカー(1L,200ml),薬サジ,スポイト,水酸化ナトリウム,フェノールフタレイン,m-ニトロフェノール,チモールフタレイン
【虹色の水の作り方】
水酸化ナトリウム0.4gを水1Lに溶かした溶液を,200mlのビーカーに100mlずつ入れます(これを6つ作ります)。
そして,それぞれのビーカーに,以下の方法で作った指示薬を2滴ずつ入れると,次のような色の溶液を作ることができます。
●赤 フェノールフタレイン1.5g+m-ニトロフェノール3.0g
●オレンジ フェノールフタレイン10.1g+m-ニトロフェノール6.0g
●黄 m-ニトロフェノール6.0g
●緑 m-ニトロフェノール6.0g+チモールフタレイン0.6g
●青 チモールフタレイン1.5g
●紫 チモールフタレイン0.4g+フェノールフタレイン0.9g





コメント